丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂 擄夝搙丂丂丂丂丂丂 丂 儕儞僋 晄巚媍側怓偺悽奅 丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂 堈丂丂丂丂丂丂丂 丂丂偁傝怓偺尒偊傞巇慻傒 丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂堈丂丂丂丂丂丂丂丂丂 偁傝丂俀倎亅俀丂丂怓偲偼 丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂 堈丂丂丂丂丂丂丂丂丂 偁傝怓偲揹巕偺晄巚媍側娭傢傝 丂丂丂丂丂丂丂丂丂丂 丂 傗傗擄丂丂丂丂丂丂丂丂偁傝 僐乕僸乕僽儗乕僋 侾 丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂 丂 徫乛堈丂丂丂丂丂丂丂丂偁傝丂丂丂丂丂丂丂丂 嬀偺嵍塃偼媡丄偱傕忋壓偼側偤丏丏丏 斀幩丄摟夁乛孅愜丄媧岝丂丂丂丂丂丂 丂丂丂 丂 丂傗傗擄乣擄丂丂丂丂丂丂 側偟 僐乕僸乕僽儗乕僋 俀 丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂 丂丂傗傗擄丂丂 丂丂丂丂丂偁傝尰幚偵尒偊傞検巕偺晄巚媍側悽奅 怓偺曄傢傞傢偗乮侾乯 丂 丂丂丂丂丂丂丂丂丂丂丂丂 丂丂丂 丂堈丂丂丂丂丂丂丂丂丂側偟 僐乕僸乕僽儗乕僋 俁 丂丂 丂丂丂 丂丂丂丂丂丂丂丂丂丂 丂丂丂堈丂丂丂丂丂丂丂 丂 側偟 壴偺怓 怓偺曄傢傞傢偗乮俀乯 丂 丂丂丂丂丂丂丂丂丂丂丂丂 丂丂堈乣傗傗擄丂丂丂丂丂 側偟 僐乕僸乕僽儗乕僋 係 丂丂 丂丂丂丂丂丂丂丂 丂丂丂丂丂丂丂傗傗擄丂丂丂丂丂丂丂 側偟 奼嶶 傑偲傔 丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂 丂丂 丂丂丂丂丂 丂丂 堈丂丂丂丂丂丂丂丂 側偟 崅暘巕偺壢妛 丂乮乫侽俆丏俋丏侾丂俶俤倂乯 丂丂丂丂丂丂丂 堈乣傗傗擄丂丂丂丂丂偁傝壢妛儘働僢僩偱偁偦傏偆 丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂堈丂丂丂丂丂丂丂丂 偁傝 丂丂丂丂乮扽巁僈僗偵傛傞悇恑乯 亅亅亅亅亅
丂丂丂怓偑尒偊傞尰徾丄怓偑曄壔偡傞尰徾偼丄偨偄傊傫墱偑怺偄傕偺偱偡丅
丂丂丂丂丂丂丂丂丂丂 Copyright (C) 2005 http://iromizu.com, all rights reserved.
乮拲丗乯 仸拲丗亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅 丂丂丂丂丂丂丂丂丂丂 Copyright (C) 2005 http://iromizu.com, all rights reserved.
偙偪傜 傪嶲徠偔偩偝偄丅妋偐偵儅僛儞僞偼偁傝傑偣傫偹丅丂丂丂丂丂丂丂丂丂丂 Copyright (C) 2005 http://iromizu.com, all rights reserved.
丂俀倎亅俀亅侾丂岝偺俁尨怓丄偊偺偖偺俁尨怓 儅僛儞僞偑娷傑傟偰偄側偄 偺偱偟傚偆偐丅丒丒丒 崿偤偰偱偒偨墿怓 偲丄 扨怓僗儁僋僩儖偺墿怓 偲偺堘偄偼壗丠 丂椙偔偛懚偠偺擑偺俈怓偑帵偝傟偰偄傑偡偑丄偊偺偖偺俁尨怓偱偁偭偨峠乮儅僛儞僞亖愒巼乯偩偗偼擑偺怓偵偼娷傑傟傑偣傫丅峠偺扨怓僗儁僋僩儖偼懚嵼偟側偄偺偱偡丅偝傑偞傑側怓傪帩偭偨壴乆 偑懚嵼偟丄愒丄烌丄墿丄惵丄巼側偳柍悢偺旝柇側怓崌偄偲嫟偵丄巹偨偪偺栚傪妝偟傑偣偰偔傟傑偡丅-3 値倣偐傜丄揹攇偲屇偽傟傞侾儊乕僩儖偐傜昐僉儘儊乕僩儖偵傕媦傇峀偄揹帴攇偺攇挿堟偺拞偱丄壜帇岝偲屇偽傟傞係侽侽乣俈侽侽値倣偲偄偆嬌傔偰嫹偄斖埻偺攇挿堟偱丄偁傟偩偗朙晉側怓傪姶偠丄壴偵堨傟偨弔偵偼丄偦偺旤偟偝傪枮媔偡傞偙偲偑偱偒傞偺偱偡丅巹偨偪偺栚偺巇慻傒丄怓傪姶偠傞巇慻傒偑偆傑偔偱偒偰偄偰偄傞桳傝擄偝傪姶偠傑偡偑丄偦傟偲摨帪偵丄偄傠偄傠側怓傪嶌傝弌偟偰偄傞壴偺曽傕丄暋嶨側壔妛斀墳傪梡偄偰怓慺傪嶌傝丄偙傟傪崿偤崌傢偣偰丄岻傒偵旝柇偵堎側傞偨偔偝傫偺怓挷傪嶌傝弌偡搘椡傪偟偰偄傞偺偱偡丅 丂丂丂丂丂丂丂丂丂丂 Copyright (C) 2005 http://iromizu.com, all rights reserved.
丂俀倎亅俁亅侾丂岝偲偼-3 値倣傪拞怱偵偟偨椞堟偵暘晍偟偰偄傑偡丅-3 値倣傛傝抁偄攇挿傪帩偭偨兞 慄偲屇偽傟傞揹帴攇偐傜丄攇挿偑侾侽侽倠倣乮廃攇悢俁倠俫倸乯偵傕媦傇挻挿攇乮倁俴俥乯偲屇偽傟傞揹帴攇傑偱偺椞堟偺偆偪丄偛偔堦晹暘傪巜偟偰屇傫偱偄傞傕偺偱丄偙偺攇挿偺堘偄偐傜揹帴攇偲偟偰偺惈幙偵堘偄偑偁傞偨傔丄偙偺傛偆偵屇傃柤傪曄偊偰偄傞偺偱偡丅僐乕僸乕僽儗乕僋 俀 傪嶲徠偔偩偝偄乯丄偙偙偱偼-1 乯偲攇挿兩乮倣乯偺娫偵偼8 乛乮係侽侽亊侾侽-9 乯亖俈丏俆亊侾侽14 乮倱-1 乯14 乮倱-1 乯丂偲側傝傑偡丅岝偐傜 椼婲偵昁梫側僄僱儖僊乕偑媧廂 偝傟丄偙傟偵傛偭偰椼婲偵昁梫側僄僱儖僊乕偵憡摉偡傞攇挿乮怳摦悢乯偺岝偑媧廂偝傟傞偙偲偲側傝傑偡丅夞揮傗怳摦偺僄僱儖僊乕儗儀儖傕峫椂偡傞偲丄婎掙忬懺偐傜椼婲忬懺偵堏傞僄僱儖僊乕偑暆傪帩偭偰偍傝丄揹巕偺慗堏僄僱儖僊乕 暆傪拞怱偲偟偰丄暆傪帩偭偨岝偺媧廂懷 偑宍惉偝傟傞偙偲偵側傝傑偡丅慗堏僄僱儖僊乕 偼丄暔幙傗尨巕偵傛偭偰摿掕偺抣偵寛傑偭偰偍傝丄暋悢偺抣傪帩偭偰偄傑偡偑丄暔幙偵屌桳偺攇挿乮怳摦悢乯偺岝 偑丄偁傞暆傪帩偭偰媧廂 偝傟傞偙偲偵側傝傑偡丅岝偺媧廂偵傛傞怓 丂埲忋偱丄怓偺尒偊傞棟桼偑偩偄傇尒偊偰偒傑偟偨丅慗堏偟傗偡偄 丄摦偒傗偡偄 偲偄偭偨惈幙偑堘偆傛偆偱偡偑丄偳偆堘偆偺偱偟傚偆丅怓偑曄傢傞 偲偄偆偙偲偼丄偙傟傑偱偵尒偰偒偨傛偆側偙偲偑傜偺壗偐偑曄傢偭偨 傜偟偄丄 僐乕僸乕僽儗乕僋乮侾乯 丂丂丂丂丂丂丂丂丂丂 Copyright (C) 2005 http://iromizu.com, all rights reserved. 亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅
嬀偺嵍塃偼媡丄偱傕忋壓偼側偤丏丏丏丂 丂丂乣丂嬀偺斀幩偺懳徧惈偼丠丂乣 丂傆偩傫偼嬀傪尒偰偄偰傕晄巚媍側偙偲偼壗傕側偄偱偡偗傟偳丄偪傚偭偲偁傞偙偲偵婥偵側傞偲丄嬀 乮 偐偑傒 乯 偼塃嵍乮傒偓傂偩傝乯傕丄忋壓乮偆偊偟偨乯傕壗傕媡乮偓傖偔乯偵偟偰偼偄傑偣傫丅 丂丂丂丂丂丂丂丂丂丂 Copyright (C) 2005 http://iromizu.com, all rights reserved. 俀倎亅俆丂丂斀幩丄摟夁乛孅愜丄媧岝 丂丂http://iromizu.com丂偵帵偡庤懕偵傛偭偰丄僷僗儚乕僪偱擖偭偰偔偩偝偄丅
丂愭傎偳丄壜帇岝偺僗儁僋僩儖偲怓偲偺娭學偵偮偄偰尒偰偒傑偟偨偑丄偙偺岝偲偼壗偱偟傚偆丅 丂偝偰丄崅峑偺暔棟偱妛傃傑偡偑丄岝偼師偺傛偆側惈幙傪帩偭偰偄傑偡丅俁 僿儕僂儉嘦偼丄偦偺拞偵惗偠偨塓偺嫮偝偑旘傃旘傃偺抣偟偐庢傞偙偲偑偱偒側偄偲偄偆丄傑偝偵検巕椡妛偺尰徾傪帵偡偲偺偙偲偱偡丅俀 壏搙偺挻揹摫偼揹巕偺嬅弅偩偗偱偼尰徾傪愢柧偱偒側偄柺偑偁傞偦偆偱偡丅乯 Copyright (C) 2005 http://iromizu.com, all rights reserved. 亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅亅俀倎亅俈丂丂 怓偺曄傢傞傢偗乮侾乯 丂丂丂丂丂丂曗彆夝愢丗丂戝偒側悢 丂 俀倎亅俉丂丂僐乕僸乕僽儗乕僋 俁 俀倎亅俋丂丂怓偺曄傢傞傢偗乮俀乯 俀倎亅侾侽丂僐乕僸乕僽儗乕僋 係 俀倎亅侾侾丂傑偲傔 丂丂俁崁 偵帵偡庤懕偵傛偭偰丄僷僗儚乕僪偱擖偭偰偔偩偝偄丅 俀倐丂崅暘巕偺壢妛 嬌傔偰嬌傔偰婓側 傕偺偵側傝傑偡丅塅拡傪宍惉偟偰偄傞暔幙偺俋俋亾偁傞偄偼堦愢偱偼俋俋丏俋亾偑僾儔僘儅偱偁傞偲尵傢傟偰偍傝丄屌懱丄婥懱偼巆傝偺偛偔傢偢偐丄塼懱偼峏偵傢偢偐側傕偺偲側傝傑偡丅暔幙偺俁懺乮亖屌懱丄塼懱丄婥懱乯側偳偲尵傢傟傑偡偑丄塅拡慡懱偱偼俁懺偺忬懺偵偁傞傕偺偼嬌傔偰彮側偔丄傎偲傫偳偼係懺栚偺乽僾儔僘儅乿側偺偱偡丅偦偟偰崅暘巕壔崌暔側偳偲偄偆傕偺偼抧媴奜偵偼傎偲傫偳側偝偦偆偱偡丅乮瑕愇偐傜傾儈僲巁偑専弌偝傟偨偲偄偆僯儏乕僗傕暦偒傑偡偟丄尨巒惗柦偼帺慠偵崌惉偝傟偨傾儈僲巁偐傜偱偒偨僞儞僷僋幙偑尦偱偁傞偲尵傢傟偰偄傑偡偺偱丄乽側偄乿偲傕尵偊側偄傛偆偱偡丅乯侾亅侾侾倎乽幍怓偺傇偳偆乿 偱庡栶傪墘偠偰偄傞丄崅暘巕壔崌暔嵽椏乽傾儖僊儞巁乿偺峔憿偵偮偄偰尒偰傒傑偟傚偆丅丂偙偺傛偆偵丄傾儖僊儞巁偼扽慺俠偺崪奿偵巁慺俷丆悈慺俫偑偮側偑傝丄偙偺婎杮宍偑孞傝曉偟偮側偑偭偰偱偒偰偄傞傕偺偱偡丅丂偙偺拞偱丂亅俠俷俷俫丂偲側偭偰偄傞晹暘偑乽巁乿偺摿挜傪帩偭偰偄傞梫場偱丄傢偢偐偱偡偑丂亅俠俷俷丂偲丂俫亄 偵揹棧偟偰巁偺惈幙傪帵偟傑偡丅丂傾儖僊儞巁僫僩儕僂儉偱偼丄偙偺悈慺俫偑僫僩儕僂儉俶倎偵抲偒姺傢偭偰丂亅俠俷俷俶倎丂偲側偭偨傕偺丄傾儖僊儞巁僇儖僔僂儉偼俀屄偺悈慺偲抲偒姺傢偭偰丂亅俠俷俷
俠倎 俷俷俠亅丂偲俀売強偺丂亅俠俷俷俫丂傪偮側偘偰偱偒偨傕偺偱偡丅 俀倐亅俀丂傾儖僊儞巁偑屌傑傞傢偗 丂傾儖僊儞巁僫僩儕僂儉偼俶倎偺揹巕懳偺榬偑侾杮側偨傔丄丂亅俠俷俷俫丂偺俫偲擖傟懼傢傞偩偗偱偟偨丅丂偙偺忬懺偱悈偵梟偐偣偽丄悈梟塼偲側偭偰偄傑偡丅丂偲偙傠偑丄愭傎偳傾儖僊儞巁僇儖僔僂儉偱尒偨傛偆偵丄僇儖僔僂儉偱偼揹巕懳偺榬偑俀杮偁傞偨傔偵丄俀売強偺丂亅俠俷俷俫婎傪僇儖僔僂儉僀僆儞乮俠倎俀亄 乯傪嫶乮攠夘乯偲偟偰寢傃偮偗傞偙偲偵側傝傑偡丅俀亄 偑攠夘偵側偭偰乮僋乕儘儞椡偱乯寢傃偮偗偰偄傑偡丅 丂僇儖僔僂儉僀僆儞俠倎俀亄 偑廫暘偵偁傞偲丄偙偺嫶偑偨偔偝傫偱偒傑偡偐傜丄堦杮偺嵔偩偭偨傾儖僊儞巁偼丄懡悢寢傃偮偄偰屌傑偭偰偄偒傑偡丅丂偙偺堦晹傪奊偵偟偨偺偑塃偺恾偱丄偙偆偟偨峔憿傪egg
box junction乮僄僢僌儃僢僋僗僕儍儞僋僔儑儞乯偲尵偄傑偡丅丂塃偺奊偲忋偺奊偼摍壙偱偡丅侾亅侾侾倎乽幍怓偺傇偳偆乿 偱墘弌偟偰偄傞偺偼丄墫壔僇儖僔僂儉悈梟塼偵傾儖僊儞巁僫僩儕僂儉梟塼傪揌壓偟偰丄偙偺egg box junction傪弖帪偵奜旂偵嶌傝丄偙偺塼揌傪屌傔偨棻偱偡丅丂帪娫偑宱偮偲丄僇儖僔僂儉僀僆儞偼撪晹偵怹摟偟偰丄拞偺曽傑偱屌傑偭偰偄偒傑偡丅丂彮偟屌傑傝巒傔偨忬懺偱庢傝弌偡偲丄僇儖僔僂儉偑傑偩廫暘抲偒姺傢偭偰偄側偄偨傔丄彮偟廮傜偐傔偺僛儕乕偺傛偆側姶偠偱偡偑丄帪娫偑宱偭偰拞偺曽傑偱屌傑傞偲丄偪傚偆偳姦揤偺傛偆偵丄傗傗屌傔偱乽偝偔偄乿姶怗偺棻偵側傝傑偡丅乽俀倐亅係丂俙倫倫倕値倓倝倶丂僗僩儘儞僠僂儉懠偵傛傞屌壔乿 偱嵞奐偡傞偙偲偵偟傑偡丅 俀倐亅俁丂崅暘巕嵽椏偄傠偄傠偄傠偄傠側怓偺壴 偑偁傝丄旤偟偄怓偺奓 偑偁傝丄朏崄傪帩偭偨壴 偑偁傝丄幚偭偨僞僱偐傜偼夎偑弌偰丄傗偑偰傑偨壴偑嶇偒傑偡偑丄偙偆偟偨怓慺丄朏崄惉暘丄敪夎婡峔偼丄慡偰惗懱撪偺怗攠乮崅暘巕偨傫傁偔偱偱偒偰偄傞傕偺偑懡偄乯側偳傪嬱巊偟偰丄捠忢偺忢壏忢埑偱偼婲偙傜側偄傛偆側壔妛斀墳傪恦懍偵恑傑偣丄惗暔偑壗偐偺栚揑傪帩偭偰乽嬯怱偟偰乿嶌傝弌偟偰偄傞傕偺側偺偱偡丅屌偔偰寉偄崅暘巕慇堐 岝偱怢弅偡傞崅暘巕慇堐 捠忢偵懚嵼偡傞偺偼忋嵍懁偺trans-傾僝儀儞僛儞偺曽偱丄偙傟偼烌愒怓傪偟偨梩忬寢徎偺暔幙偱偡丅 丂忋偺恾偵帵偟偨傛偆偵丄偙偺trans-傾僝儀儞僛儞偵俁侾俁値倣晅嬤偺巼奜岝傪摉偰傞偲丄暘巕偺宍懺偑曄傢傝丄忋塃懁偺cis-傾僝儀儞僛儞偵曄傢傝傑偡丅丂cis-傾僝儀儞僛儞偼係俁俇値倣晅嬤偺惵怓壜帇岝傪摉偰傞偐丄壛擬偡傞偲丄嵞傃尦偺trans-傾僝儀儞僛儞偵栠傝傑偡丅巁慺傪傛傝暘偗傞崅暘巕枌 偐傇偭偨傝偟側偄 傛偆偵拲堄偟偰偔偩偝偄丅丂摟夁偡傞巁慺偺 愨懳検 偑丄屇媧偵昁梫側検傪 慡偔枮偨偝側偄 偺偱丄屇媧偱偒側偔側傝傑偡丅乯丂崅暘巕枌傪巁慺偑捠夁偡傞偲偄偆偺偼丄崅暘巕枌偺嵽椏偺拞偵巁慺偑堦扷梟偗偰丄斀懳懁偐傜弌偰偔傞偲偄偆傛偆偵棟夝偟偨曽偑暘偐傝堈偄偱偟傚偆丅俁 乯傪偪傝偽傔偨峔憿傪帩偭偰偄傑偡丅丂偙偺嵽椏偼巁慺偺慖戰摟夁摿惈偵桪傟偰偍傝丄寚揰偺嫮搙傪暿偺嵽椏枌偱曗偭偰丄堛椕梡巁慺惢憿婍傗丄巁慺摟夁惈僜僼僩僐儞僞僋僩儗儞僘丄擱椏摍偺杊敋廩揢梡拏慺惢憿丄敿摫懱娭楢偺拏慺嫙媼側偳偵棙梡偝傟偰偄傑偡丅 乣乣乣乣乣乣乣乣乣乣乣乣乣乣乣乣乣乣乣乣乣乣乣乣乣乣乣乣乣乣乣乣乣乣乣乣乣 俀倐亅係丂俙倫倫倕値倓倝倶丂僗僩儘儞僠僂儉懠偵傛傞屌壔 丂丂丂亅亅亅丂梫揰乮偐傫偨傫偵偄偆偲乯丂亅亅亅 僇儖僔僂儉 僀僆儞乮俠倎俀亄 乯偲傾儖僊儞巁 僫僩儕僂儉偱丄塼懱偐傜偙偺傛偆側屌宍暔偑偱偒傞偙偲偼椙偔抦傜傟偰偍傝丄偄傠偄傠側恾彂丄弌斉暔偵婰嵹偝傟偰偄傑偡丅偟偐偟丄偙偙偱偼偙傟偩偗偱廔傢偭偰偼偍傕偟傠偔偁傝傑偣傫丅 丂偣偭偐偔乽壢妛偱偁偦傏偆乿 偲偟偰偄傞傢偗偱偡偐傜丄傕偆堦偮晜偐傫偱偒偨媈栤偺摎偊傪幚尡偱妋擣偟偰傒傑偟傚偆丅丂廃婜棩昞偱摨偠楍 偵埵抲偡傞儅僌僱僔僂儉 僀僆儞乮俵倗俀亄 乯丄偙傟偼摛晠傪屌傔傞乽偵偑傝乿偵娷傑傟偰偄偨傝丄壓嵻偵棙梡偝傟偨傝丄傑偨堦曽偱偼丄怉暔偺梩椢慺偺拞怱傪側偟偰偄傞廳梫側尦慺偱偡丅丂偙偺儅僌僱僔僂儉 僀僆儞乮俵倗俀亄 乯傗丄摨偠廃婜棩昞偺廲拠娫偺僗僩儘儞僠僂儉 僀僆儞乮俽倰俀亄 乯傪僇儖僔僂儉僀僆儞偺戙傢傝偵梡偄偨応崌偳偆側傞偐尒偰傒傑偟傚偆丅俉俋 俽倰丆俋侽 俽倰乯偑弌偰偔傞偙偲偱傕抦傜傟偰偍傝丄偙偪傜偺摨埵懱偼曻幩擻傪懷傃偰桳奞偱偡偑丄堦斒偵擖庤壜擻側僗僩儘儞僠僂儉壔崌暔乮俉俉 俽倰丄俉俇 俽倰丄俉俈 俽倰丄俉係 俽倰偺偦傟偧傟俉俀丏俇亾丆 俋丏俋亾丆 俈丏侽亾丄 侽丏俆亾偺崿崌暔乯偼曻幩擻傪帩偭偰偄傑偣傫丅丂乮偙偆偟偨俉俉 俽倰埲奜偺尨巕傕娷傑傟偰偄傞偨傔丄僗僩儘儞僠僂儉偺尨巕検偼俉俈丏俇俀偲偄偆拞搑敿抂側悢抣偵側偭偰偍傝丄椺偊偽巁慺乮亖侾俇丏侽侽乯偺傛偆偵俉俉丏侽侽傄偭偨傝偵偼側傜側偄偺偱偡丅乯俀亄 僀僆儞偵傛偭偰屌壔丂丂丂丂丂丂丂丂丂俠倎俀亄 僀僆儞偵傛偭偰屌壔摨偠傛偆偵俀杮偺榬傪帩偮摵 僀僆儞乮俠倳俀亄 乯傗僯僢働儖 僀僆儞乮俶倝俀亄 乯丄儅儞僈儞 僀僆儞乮俵値俀亄 乯丄揝 僀僆儞乮俥倕俀亄 乯傪梡偄偨応崌偼偳偆側傞偱偟傚偆偐丅廃婜棩昞偱偼慡偔堘偆楍偵埵抲偟偰偄傑偡偑丄偳偺傛偆側惈幙偑億僀儞僩側偺偱偟傚偆偐丅揝僀僆儞偱傕俁壙 偺傕偺乮俥倕俁亄 )傕偁傝傑偡偹丅偙傟傪梡偄偨応崌偼偳偆偱偟傚偆丄屌傑傞偱偟傚偆偐丅揝偺俁杮偺榬偵俁杮偺傾儖僊儞巁偑寢崌偟偰峏偵崅暘巕偲側偭偰屌壔偡傞偺偱偟傚偆偐丅峏偵俁壙偺嬥懏僀僆儞戙昞慖庤傾儖儈僯僂儉 僀僆儞乮俙倢俁亄 乯偱偼偳偆偱偟傚偆偐丅僠僞儞 僀僆儞乮俿倝係亄 乯偱偼僠僞儞尨巕傪拞怱偵係杮偺傾儖僊儞巁偑寢崌偡傞偱偟傚偆偐丅僇儕僂儉 偲摨偠傛偆側丄榬偑侾杮偺嬥懏僀僆儞偱偡丅丂摵偼捠忢俀壙偺僀僆儞傪宍惉偟傑偡偑丄巁壔忬懺偵傛偭偰偼侾壙偺忬懺傪偲傝傑偡丅丂偙偺傛偆側梕堈偵巁壔乛娨尦偝傟傞惈幙傪帩偭偰偄傞偙偲偐傜丄巁壔娨尦偺怗攠偲偟偰巊偆偙偲傕偁傝傑偡丅丂偙偙偱偼丄弮悎偵堦壙偺摵僀僆儞偩偗傪摼傞偙偲偼擄偟偄偺偱丄廃婜棩昞偱摵偲摨偠宯楍偱偡偑丄捠忢偺忬懺偱偼侾壙偺僀僆儞嬧 偱偼偳偆側傞偐帋偟偰傒傑偟傚偆丅丂僫僩儕僂儉側偳偲摨偠傛偆偵丄傾儖僊儞巁偺崅暘巕偵堦杮偺榬偱傇傜壓偑傞偩偗側偺偱丄屌傑傜側偄偲偄偆偺偑摎偊偱偟傚偆偐丠丏丏丏Copyright (C) 2005 http://iromizu.com, all rights reserved.

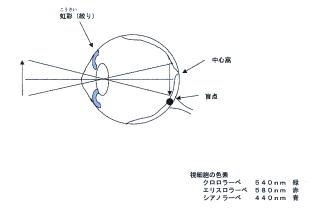 丂巹偨偪偺栚偼丄奜奅偺岝傪庢傝擖傟丄捠夁偡傞岝検傪挷愡偟丄儗儞僘傪捠偟偰徟揰傪挷愡偟丄岝傪栐枌忋偵憸偲偟偰搳塭偟丄帇妎恄宱偵傛傝恄宱偺怣崋偵曄姺偟丄擼偵憲偭偰忣曬傪張棟偟丄暔偺宍傗怓側偳傪擣幆偟偰偄傑偡丅
丂巹偨偪偺栚偼丄奜奅偺岝傪庢傝擖傟丄捠夁偡傞岝検傪挷愡偟丄儗儞僘傪捠偟偰徟揰傪挷愡偟丄岝傪栐枌忋偵憸偲偟偰搳塭偟丄帇妎恄宱偵傛傝恄宱偺怣崋偵曄姺偟丄擼偵憲偭偰忣曬傪張棟偟丄暔偺宍傗怓側偳傪擣幆偟偰偄傑偡丅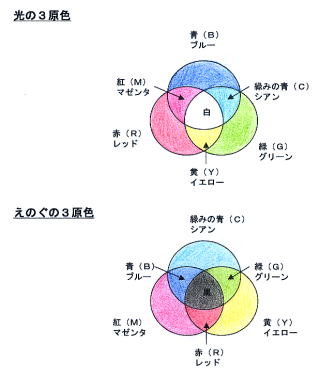 丂塃偺奊偼丄
丂塃偺奊偼丄
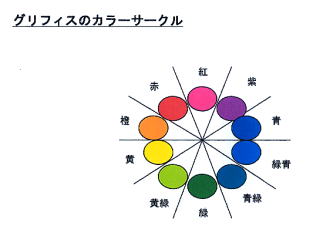 丂墿怓偺偊偺偖偲惵偺偊偺偖傪崿偤傞偲丄崟偵側傝傑偡偑丄偙傟偼師偺傛偆偵愢柧偝傟傑偡丅
丂墿怓偺偊偺偖偲惵偺偊偺偖傪崿偤傞偲丄崟偵側傝傑偡偑丄偙傟偼師偺傛偆偵愢柧偝傟傑偡丅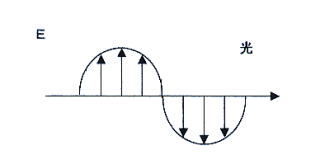 丂塃偺恾偱侾廃婜偑偦傟偧傟係侽侽値倣偺岝傪巼丄俈侽侽値倣偺傕偺傪愒偲姶偠傑偡丅
丂塃偺恾偱侾廃婜偑偦傟偧傟係侽侽値倣偺岝傪巼丄俈侽侽値倣偺傕偺傪愒偲姶偠傑偡丅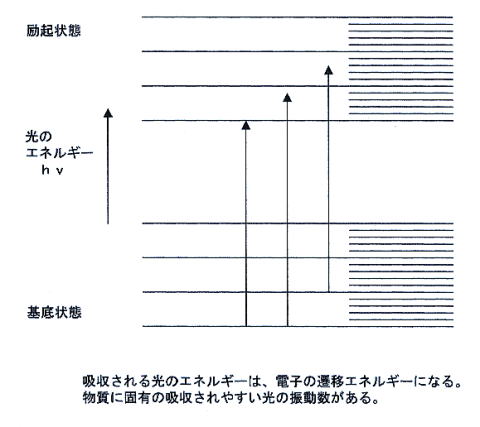




 丂僇儖僔僂儉僀僆儞俠倎俀亄偑廫暘偵偁傞偲丄偙偺嫶偑偨偔偝傫偱偒傑偡偐傜丄堦杮偺嵔偩偭偨傾儖僊儞巁偼丄懡悢寢傃偮偄偰屌傑偭偰偄偒傑偡丅丂偙偺堦晹傪奊偵偟偨偺偑塃偺恾偱丄偙偆偟偨峔憿傪egg
box junction乮僄僢僌儃僢僋僗僕儍儞僋僔儑儞乯偲尵偄傑偡丅丂塃偺奊偲忋偺奊偼摍壙偱偡丅
丂僇儖僔僂儉僀僆儞俠倎俀亄偑廫暘偵偁傞偲丄偙偺嫶偑偨偔偝傫偱偒傑偡偐傜丄堦杮偺嵔偩偭偨傾儖僊儞巁偼丄懡悢寢傃偮偄偰屌傑偭偰偄偒傑偡丅丂偙偺堦晹傪奊偵偟偨偺偑塃偺恾偱丄偙偆偟偨峔憿傪egg
box junction乮僄僢僌儃僢僋僗僕儍儞僋僔儑儞乯偲尵偄傑偡丅丂塃偺奊偲忋偺奊偼摍壙偱偡丅



















